新規CPFC(細胞培養加工施設)の立ち上げやGCTP査察に向けた準備において、最も頭を悩ませるのがSOP(標準作業手順書)体系の構築ではないでしょうか。
膨大な数の手順書を整合性を保ちながら整備し、かつ法令に適合させる作業は、非常に骨の折れる業務です。しかし、堅牢なSOP体系は、再生医療等製品の品質を担保し、患者様の安全を守るための「要」となります。
本記事では、再生医療の現場で求められるGCTP準拠のSOP体系構築について、その全体像から具体的な作成ステップ、運用管理のポイントまでを体系的に解説いたします。
実務で直面する課題を解決し、効率的かつ確実な文書管理体制を築くための一助となれば幸いです。
CPFC運営におけるSOP体系構築の結論:GCTP適合と運用効率の両立

CPFC運営において、SOP体系の構築は単なる書類作成ではありません。それは、組織全体が法令を遵守し、かつ効率的に業務を遂行するための「基盤作り」に他なりません。
目指すべきは、GCTP省令への完全な適合と、現場スタッフが迷いなく動ける運用効率の両立です。ここでは、そのために必要な核となる考え方について解説いたします。
製品標準書を頂点とした整合性の取れた階層構造の確立
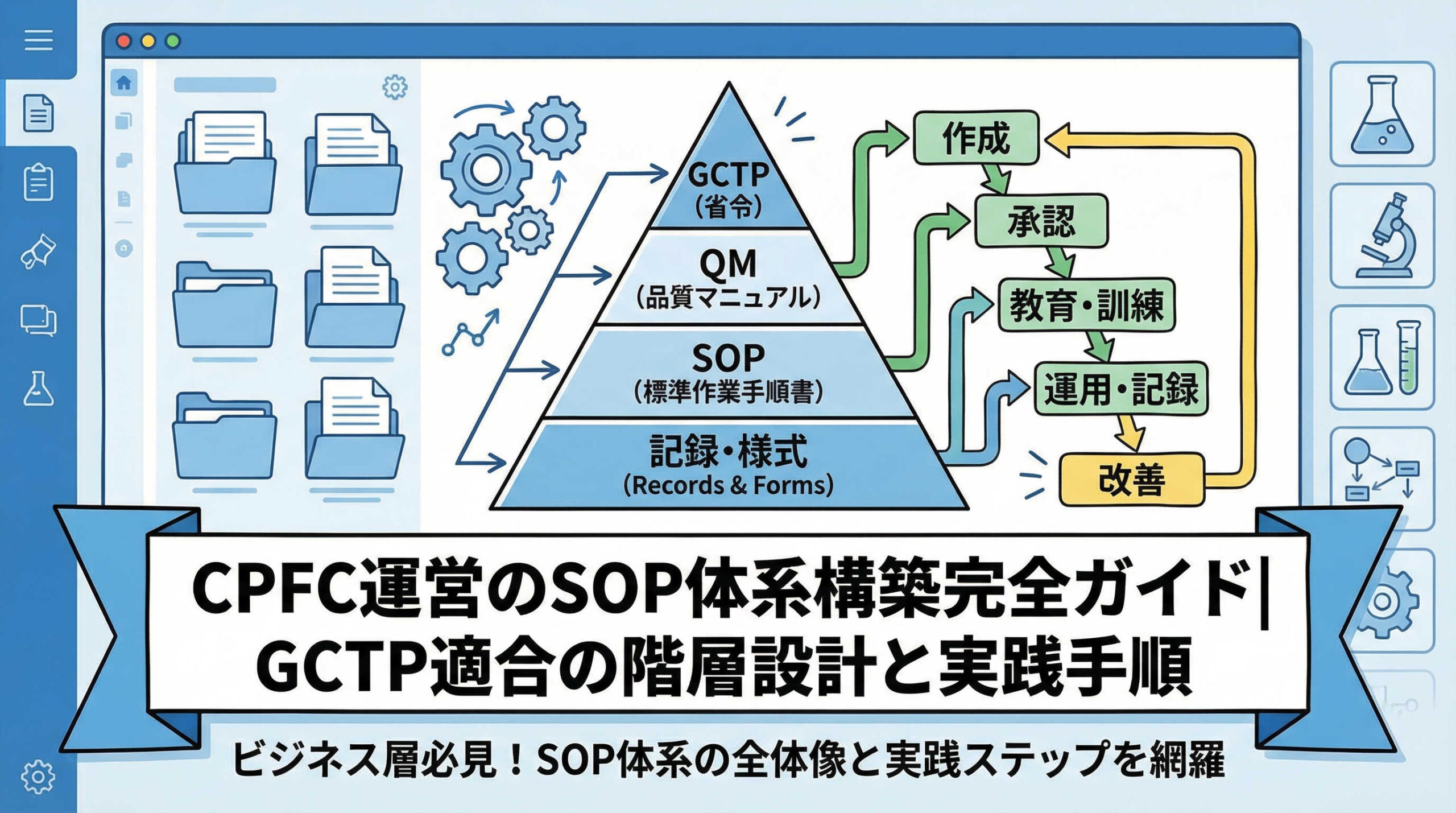
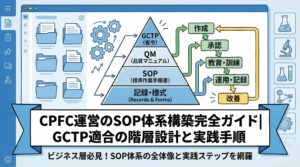
SOP体系を構築する際、最も重要なのは「製品標準書」を頂点としたピラミッド型の階層構造を確立することです。製品標準書には、その製品の製造方法や品質管理の全貌が記載されており、すべての下位文書はこの内容と矛盾してはなりません。
上位文書(基準書など)から下位文書(SOP、記録様式)へと、論理的に整合性が取れている状態を作ることで、変更管理や逸脱対応がスムーズになります。文書間のリンクが切れていると、一部の改訂が全体に波及せず、現場での混乱や法令違反のリスクを招く原因となりますので、設計段階での構造化が極めて重要です。
製造部門と品質部門の役割分担を明確化した文書体系
GCTP省令では、製造部門と品質保証部門の独立性が強く求められます。SOP体系においても、この役割分担を明確に反映させる必要があります。
具体的には、「誰が実施し、誰が確認し、誰が承認するのか」という権限と責任の所在を、文書上で明確に区分します。
例えば、製造に関するSOPは製造部門が作成し、品質保証部門が照査・承認するといったフローを規定します。このように文書体系自体に牽制機能を組み込むことで、組織としてのガバナンスが強化され、自己点検や監査においても高い評価を得られる体制へとつながります。
査察対応を見据えたトレーサビリティの確保
査察において最も厳しくチェックされるポイントの一つが「トレーサビリティ(追跡可能性)」です。SOP体系を構築する際は、最終製品から原材料、製造記録、試験記録、そして実施した担当者の教育訓練記録まで、双方向に追跡できる仕組みを埋め込む必要があります。
記録様式(ログブックやバッチレコード)には、必ず参照したSOPの番号や版数を記載する欄を設けるなど、文書間の紐付けを徹底しましょう。これにより、万が一のトラブル発生時にも、どの手順に基づいて作業が行われたかを即座に特定でき、迅速な対応が可能となります。
なぜCPFCでは緻密なSOP体系の構築が不可欠なのか

再生医療等製品は、その性質上、従来の医薬品以上に厳格な管理が求められます。なぜCPFCにおいて、これほどまでに緻密で体系的なSOP構築が不可欠なのでしょうか。
それは、ヒトの細胞を取り扱うという特殊性と、製品の品質がプロセスそのものに依存するという特徴があるからです。ここでは、SOP体系構築の重要性を4つの視点から深掘りします。
再生医療等製品の製造管理及び品質管理の基準(GCTP省令)への法的適合
まず第一に、GCTP省令(再生医療等製品の製造管理及び品質管理の基準に関する省令)への法的適合が必須条件となります。GCTPは、製造所の構造設備から製造管理、品質管理、衛生管理に至るまで、詳細な基準を定めています。
これらの要求事項を満たしていることを客観的に証明する唯一の手段が「文書化」です。口頭での伝承や暗黙の了解は、規制当局には一切通用しません。SOP体系は、施設が法令を遵守して運営されていることを示す「証拠」であり、事業継続のためのライセンスそのものと言えるでしょう。
担当者に依存しない均質な製造品質の維持
細胞培養などの手技は、担当者の技術レベルや癖によって結果にバラつきが生じやすい工程です。しかし、医薬品としての品質を担保するためには、「誰がいつ作業しても同じ結果が得られる」ことが求められます。
詳細かつ具体的なSOPが存在することで、個人の経験や勘に頼る部分を極小化し、作業の標準化を図ることができます。これは、熟練者のノウハウを形式知化し、組織全体の技術レベルを底上げすることにも繋がります。均質な品質維持は、製品の有効性と安全性を保証する土台となります。
逸脱発生時の原因究明とCAPA(是正・予防措置)の迅速化
製造過程で何らかの異常(逸脱)が発生した場合、その原因を特定し、適切な是正・予防措置(CAPA)を講じる必要があります。この際、しっかりとした基準(SOP)がなければ、「何が通常と異なっていたのか」を比較・検証することができません。
SOPは正常な状態を定義したものであり、そこからのズレを検知するための物差しです。緻密なSOP体系があれば、逸脱の原因が手順の不備なのか、職員のミスなのか、原材料の問題なのかを論理的に切り分けることができ、再発防止策の精度を高めることができます。
実地調査(査察)における文書提示のスムーズな対応
PMDA(医薬品医療機器総合機構)や都道府県による実地調査(査察)では、限られた時間内で膨大な資料を確認されます。この際、SOPが体系的に整理されていなければ、調査官が求める文書を即座に提示できず、管理体制に疑念を持たれる可能性があります。
「必要な文書が、あるべき場所に、最新の状態で保管されている」ことは、査察対応の基本です。整理されたSOP体系は、調査官に対して「管理が行き届いている施設である」というポジティブな心証を与え、スムーズな査察進行を助ける強力な武器となります。
GCTPに準拠した文書階層構造(ドキュメントピラミッド)の設計

SOP体系を構築する際は、文書のレベルに応じた階層構造(ドキュメントピラミッド)を意識することが大切です。すべての文書をフラットに並べるのではなく、上位概念から具体的な作業指示へとブレイクダウンしていく構成にします。
この階層構造を明確にすることで、文書間の関係性が整理され、管理や改訂が容易になります。GCTP準拠の典型的な4階層モデルについて見ていきましょう。
第1階層:品質マニュアル・製造管理基準書・品質管理基準書・衛生管理基準書
ピラミッドの頂点に位置するのが、組織全体の品質方針や製造管理の基本ルールを定めた上位文書です。「品質マニュアル」を最上位とし、その下にGCTP省令で作成が義務付けられている「製造管理基準書」「品質管理基準書」「衛生管理基準書」などが配置されます。
これらは「何をするか(What)」や「誰が責任を持つか(Who)」といった方針を示すものであり、頻繁に変更されるものではありません。すべての下位文書は、これらの基準書の方針に従って作成される必要があります。
第2階層:標準作業手順書(SOP)
第2階層は、具体的な業務の手順を記述した「標準作業手順書(SOP)」です。ここでは、基準書で定められた方針を、実際の業務フローとして「どのように実施するか(How)」を記述します。
例えば、「細胞培養SOP」や「クリーンルーム清掃SOP」などがこれに該当します。SOPは、作業者が迷わずに業務を遂行できるよう、手順をステップごとに具体的に記述する必要があります。また、使用する機器や試薬、注意事項なども明記し、実務のガイドラインとしての役割を果たします。
第3階層:作業指図書・記録様式(フォーマット)・ログブック
第3階層は、SOPに基づいて日々の作業で使用する「作業指図書」や、結果を記録する「記録様式(フォーマット)」、機器の使用履歴を残す「ログブック」などです。これらは現場で最も頻繁に利用される文書です。
SOPが「教科書」だとすれば、これらは「ノート」や「テスト用紙」にあたります。記録様式は、記入漏れや記載ミスを防ぐため、チェックリスト形式を採用したり、記入欄を明確に枠で囲ったりするなど、ユーザビリティを考慮した設計が求められます。
外部文書:公定書・機器取扱説明書・試薬添付文書の管理位置づけ
社内で作成する文書以外にも、日本薬局方などの「公定書」、機器メーカーの「取扱説明書」、試薬の「添付文書(COA含む)」なども、CPFC運営において重要な外部文書として管理する必要があります。
これらはSOPの中で参照先として引用されることが多いため、常に最新版を維持管理する仕組みが必要です。外部文書管理リストを作成し、改訂状況を定期的にチェックする手順をSOPに組み込んでおくことで、意図せず古い情報に基づいて作業してしまうリスクを回避できます。
CPFC運営に必要なSOPの具体的カテゴリーと網羅すべき項目

CPFCの運営には多岐にわたる業務が含まれており、それら全てを網羅するSOPが必要です。抜け漏れを防ぐためには、業務をカテゴリーごとに分類し、リストアップしていくアプローチが有効です。
ここでは、GCTPの要求事項に基づき、CPFC運営において整備しておくべきSOPの主要なカテゴリーと、その具体的な項目例をご紹介します。
構造設備および製造用機器の保守点検に関するSOP
ハードウェアの管理は品質確保の前提です。製造を行う部屋(構造設備)や、インキュベーター、安全キャビネットなどの製造用機器に関するSOPを整備します。
具体的には、空調システムの点検、HEPAフィルターの性能確認、機器の始業前点検・定期点検、校正(キャリブレーション)の手順などが含まれます。故障時の対応フローや、緊急時の連絡体制についても定めておくことが重要です。
職員の衛生管理および更衣・手洗い手順に関するSOP
細胞にとって最大のリスク要因の一つは「人」由来の汚染です。職員の衛生管理に関する厳格なルール作りが求められます。
健康状態の確認方法(体調不良時の報告ルール)、更衣室での更衣手順、手洗い・消毒の方法、作業衣の洗濯・滅菌管理などを詳細に定めます。特に更衣手順は、写真や図解を用いた視覚的なSOPにすることで、正しい手順の定着を図ることができます。
無菌操作およびクリーンルーム入退室管理に関するSOP
CPFCの核心部分である無菌操作エリアの管理です。クリーンルームへの入退室ルール、物品の搬入出方法(パスボックスの使用手順)、室圧や温湿度のモニタリング基準などを定めます。
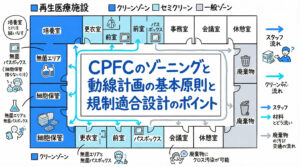
また、無菌操作そのものの基本動作(Aseptic Technique)や、環境モニタリング(落下菌、浮遊菌、表面付着菌の測定)の手順もこのカテゴリーに含まれます。交差汚染防止のための動線管理も文書化しておきましょう。
原材料・資材の受入試験および保管管理に関するSOP
質の高い製品は、質の高い原材料から生まれます。培地、試薬、消耗品などの受入時に行う確認項目(外観、使用期限、ロット番号など)や、試験の手順を定めます。
また、保管管理については、適切な温度管理(冷蔵、冷凍、室温)、在庫管理方法、先入れ先出しのルールなどを規定します。不適合品が誤って使用されないよう、隔離・廃棄の手順も明確にする必要があります。
細胞加工物の製造工程および工程内管理に関するSOP
実際の細胞加工プロセスを規定する、最もボリュームのある部分です。細胞の受入、分離、培養、継代、回収、洗浄、充填といった一連の流れを工程ごとにSOP化します。
各工程での判定基準(細胞数、生存率、外観など)や、工程内管理試験(IPC)の実施タイミングも明記します。複数の製品を扱う場合は、取り違え防止のための識別管理手順も極めて重要になります。
品質試験および検体の管理に関するSOP
最終製品の出荷可否を判断するための品質試験に関するSOPです。無菌試験、マイコプラズマ否定試験、エンドトキシン試験、ウイルス否定試験、性状試験、確認試験などの手順を網羅します。
検体のサンプリング方法、検体の保管・輸送条件、外部検査機関へ委託する場合の管理手順なども含めます。試験結果の判定基準と、規格外(OOS)となった場合の処理手順も定めておく必要があります。
逸脱管理・変更管理・バリデーションに関するSOP
品質システム(PQS)を機能させるための管理手順です。予定外の事象が起きた際の「逸脱管理」、手順や設備を変更する際の「変更管理」、プロセスや洗浄等が適切であることを検証する「バリデーション」に関するSOPです。
これらは日常的な作業手順とは異なりますが、GCTP運用の中核をなすプロセスです。リスク評価の手法や、承認フローを明確に規定し、形骸化しない運用ルールを定めることが肝要です。
教育訓練および職員の認定制度に関するSOP
SOPがいかに完璧でも、それを実行する職員にスキルがなければ意味がありません。職員の教育訓練計画の策定、実施、評価、記録に関する手順を定めます。
特に、無菌操作などの重要工程については、個人のスキルを評価し、作業への従事を許可する「認定制度」の運用手順を含めることが推奨されます。教育訓練の有効性評価や、再教育の基準についても定めておきましょう。
ゼロから始めるSOP体系構築の具体的ステップ

SOP体系の全体像が見えてきたところで、実際にゼロから構築を進めるための具体的なステップを解説します。
闇雲に書き始めるのではなく、現状分析から入り、骨子を固めてから細部を作り込むことで、手戻りの少ない効率的な構築が可能になります。以下の6つのステップを参考に進めてみてください。
ステップ1:製造販売承認書(または届出書)とGCTP省令のギャップ分析
最初のステップは、作成すべきSOPの要件定義です。承認された「製造販売承認書(または届出書)」の内容を精査し、そこで約束された製造方法や試験方法を洗い出します。
同時に、GCTP省令の条文と照らし合わせ、法令上求められる手順が網羅されているかを確認する「ギャップ分析」を行います。この段階で不足している項目をリストアップし、SOP作成リスト(マスタープラン)を作成することが、全体工程の羅針盤となります。
ステップ2:プロセスフロー図(PFD)による全作業工程の洗い出し
次に、実際の作業の流れを可視化します。原材料の搬入から製品の出荷に至るまでの全工程を、プロセスフロー図(PFD)として書き出してみましょう。
フロー図にすることで、工程の繋がりや、物と人の動きが明確になります。「ここで検体を取る」「ここで記録をつける」といった詳細なアクションをフロー上にプロットしていくことで、必要なSOPや記録様式の抜け漏れに気づくことができます。
ステップ3:リスクアセスメントに基づく重要管理点(CCP)の特定
すべての工程が同じ重要度を持っているわけではありません。品質に重大な影響を与える工程を特定するために、リスクアセスメントを実施します。
例えば、無菌操作のステップや、細胞の特性を決定づける培養工程などは、特に厳密な管理が求められる「重要管理点(CCP)」となります。リスクの高い工程については、より詳細な手順の記述や、ダブルチェックの導入などをSOPに盛り込み、リスクを低減させる設計を行います。
ステップ4:SOPドラフトの作成と現場シミュレーションによる検証
構成が固まったら、実際にSOPのドラフト(草案)を作成します。ここで重要なのは、机上の空論にしないことです。作成したドラフトを片手に、現場で実際の動きをシミュレーション(模擬動作)してみましょう。
「手順の順序に無理がないか」「記録を書くタイミングは適切か」「必要な機材が手元にあるか」などを確認します。現場スタッフの意見を積極的に取り入れ、実用的で無理のない手順へとブラッシュアップしていくプロセスが不可欠です。
ステップ5:文書番号の採番ルール決定と文書マスターの作成
文書が増えてくると管理が煩雑になります。検索性や管理効率を高めるために、体系的な文書番号の採番ルール(ナンバリングシステム)を決定します。
例えば、「SOP-MFG-001(製造部門の001番)」のように、文書種別、部門、連番などを組み合わせたルールが良いでしょう。そして、全文書の番号、タイトル、版数、制定日などを一覧化した「文書マスター(管理台帳)」を作成し、全体像を常に把握できる状態にします。
ステップ6:責任者による承認・制定および関係者への周知徹底
SOPが完成したら、製造管理者や品質保証責任者などの責任者による正式な承認を得て、制定します。しかし、制定して終わりではありません。最も重要なのは、そのSOPを使用するスタッフへの周知徹底(教育訓練)です。
新しいSOPの内容を説明し、理解度を確認した上で、教育訓練記録を残します。スタッフ全員がSOPの内容を理解し、遵守できる状態になって初めて、そのSOPは「有効」なものとして運用開始(施行)されます。
運用フェーズにおけるSOPライフサイクルマネジメント

SOPは一度作れば終わりという恒久的なものではありません。技術の進歩、法規制の改正、あるいは日々の業務改善に合わせて、常に進化させていくべき「生き物」です。
運用フェーズにおいては、SOPの鮮度と正当性を保つためのライフサイクルマネジメント(管理サイクル)が重要になります。ここでは、運用中に注意すべきポイントについて解説します。
定期的な見直しと改訂プロセスのルール化
SOPが実態と乖離することを防ぐため、定期的な見直しの時期をあらかじめ定めておきましょう(例:1年に1回など)。また、逸脱や変更管理が発生した際には、関連するSOPを随時見直す必要があります。
改訂を行う際は、単に書き換えるのではなく、「改訂理由」と「変更箇所」を明確にし、履歴として残すプロセスをルール化します。これにより、文書の変遷を追跡でき、なぜその変更が行われたのかという経緯を後から確認することができます。
旧版文書の回収と最新版の配布管理徹底
SOPを改訂した際、最も恐ろしいミスは、現場で「旧版」が使い続けられることです。これを防ぐために、最新版の配布と同時に、旧版を確実に回収・廃棄(または無効化して保管)する手順を徹底します。
配布先管理リストを用いて、誰にどのコピーを渡したかを把握し、回収漏れがないように管理します。現場には常に最新版のみが存在する環境を作ることが、誤使用防止の鉄則です。
紙媒体と電子媒体のハイブリッド管理における注意点
近年は電子化が進んでいますが、現場では紙の記録用紙を使用し、原本管理は電子で行うといった「ハイブリッド管理」のケースも多く見られます。この場合、紙と電子の整合性確保に注意が必要です。
例えば、紙の記録用紙をスキャンして電子保存する場合、原本としての正本はどちらにするのかを定義しておく必要があります。また、手書き署名の扱いなど、データの完全性(Data Integrity)を損なわないような運用ルールを明確にしておきましょう。
文書管理システム(DMS)導入による効率化の検討
SOPの数が増え、版数管理が複雑になってきた場合は、文書管理システム(DMS)の導入を検討するのも一つの手です。DMSを導入することで、承認フローの電子化、版数管理の自動化、配布・回収の効率化が可能になります。
また、検索性が向上し、必要な情報にすぐにアクセスできるようになるため、業務効率も大幅に改善します。導入コストはかかりますが、人的ミス(ヒューマンエラー)のリスク低減と管理工数の削減効果を考慮すれば、十分な投資価値があると言えるでしょう。
まとめ

CPFC運営におけるSOP体系の構築は、法令順守のためだけに行う義務的な作業ではありません。それは、組織全体に「品質文化(Quality Culture)」を根付かせ、患者様に安全で高品質な再生医療等製品を届けるための揺るぎない土台作りです。
本記事で解説した階層構造の設計、網羅的な項目の整備、そして運用フェーズでの継続的な改善サイクルを実践することで、査察にも自信を持って対応できる堅牢な体制が築けるはずです。
道のりは平坦ではありませんが、一つひとつの手順書に込められた想いが、最終的には患者様の笑顔へと繋がっています。まずは現状のギャップ分析から、着実な一歩を踏み出してみてください。
CPFC運営に必要なSOP体系の構築についてよくある質問

CPFC運営やSOP構築に関して、現場担当者からよく寄せられる質問をまとめました。実務の参考としてお役立てください。
-
SOPはどのくらいの頻度で見直すべきですか?
- 基本的には1年に1回の定期レビューを推奨します。ただし、GCTP省令の改正、製造プロセスの変更、逸脱発生時の是正措置などがあった場合は、その都度速やかに見直しと改訂を行う必要があります。
-
紙媒体と電子媒体、どちらで管理すべきですか?
- 規模や予算によりますが、近年は電子管理が主流になりつつあります。ただし、電子管理システムを導入する場合は、システムのバリデーション(CSV)やデータの完全性(Data Integrity)の確保が必要です。立ち上げ初期は紙媒体で運用し、軌道に乗ってから電子化を検討するのも一つの方法です。
-
SOPの作成は誰が担当するのが最適ですか?
- 実際にその作業を行う現場の担当者が原案を作成し、部門責任者が確認、品質保証責任者が承認するという流れが理想的です。現場の実情を知らない人が作成すると、実務とかけ離れた使いにくいSOPになりがちです。
-
外部のコンサルタントに依頼するメリットは何ですか?
- GCTPの解釈や査察のトレンドなど、専門的な知見に基づいたアドバイスが得られる点です。また、ゼロから体系を構築する際の時間短縮や、第三者視点でのギャップ分析によるリスク低減も大きなメリットと言えます。
-
SOPと作業指図書の違いは何ですか?
- SOPは「標準的な手順」を定めたマニュアル(教科書)であり、作業指図書はSOPに基づいて特定の製造ロットに対して「実施を指示」する文書(指示書)です。作業指図書には、そのロット固有の製造番号や使用する原材料のロットなどを記載し、製造記録としての役割も兼ねることが一般的です。